Hidrokarbon
Pada awalnya oleh Karl Wilhelm Scheele senyawa-senyawa menjadi dua kelompok, yaitu Senyawa organik dan anorganik. Senyawa organik adalah senyawa yang dihasilkan oleh makhluk hidup, sedangkan Senyawa anorganik adalah senyawa yang dihasilkan oleh benda mati.
Pada tahun 1807, Jons Jacob Berzelius (1779 – 1848) menyatakan teori vis vitalis, yaitu bahwa senyawa-senyawa organik hanya dapat dibuat di dalam tubuh makhluk hidup dengan bantuan daya hidup (vis vitalis), sehingga menurutnya tidak mungkin senyawa organik dibuat di laboratorium dengan menggunakan bahan senyawa anorganik.
Kedua teori tersebut masih terus dipegang hingga abad ke-19 karena belum pernah ada senyawa organik yang dibuat di laboratorium. Sampai kemudian Friederich Wohler (1800 – 1882) berhasil menumbangkan teori sebelumnya. Friederich Wohler yang juga murid Berzelius berhasil menyintesis senyawa organik. Senyawa tersebut adalah urea (yang biasa dihasilkan dari urine makhluk hidup) dengan menggunakan zat anorganik, yaitu dengan mereaksikan perak sianat dengan amonium klorida membentuk amonium sianat.
A. Keunikan Atom Karbon
Atom karbon mempunyai nomor atom 6, sehingga dalam sistem periodik terletak pada golongan IVA dan periode 2. Keadaan tersebut membuat atom karbon mempunyai beberapa keistimewaan sebagai berikut.
1. Atom Karbon Memiliki 4 Elektron Valensi
Berdasarkan konfigurasi keenam elektron yang dimiliki atom karbon didapatkan bahwa elektron valensi yang dimilikinya adalah 4. Untuk mencapai kestabilan, atom ini masih membutuhkan 4 elektron lagi dengan cara berikatan kovalen. Tidak ada unsur dari golongan lain yang dapat membentuk ikatan kovalen sebanyak 4 buah dengan aturan oktet.
2. Atom Unsur Karbon Relatif Kecil
Ditinjau dari konfigurasi elektronnya, dapat diketahui bahwa atom karbon terletak pada periode 2, yang berarti atom ini mempunyai 2 kulit atom, sehingga jari-jari atomnya relatif kecil. Hal ini menyebabkan ikatan kovalen yang dibentuk relatif kuat dan dapat membentuk ikatan kovalen rangkap.
3. Atom Karbon Dapat Membentuk Rantai Karbon
Keadaan atom karbon yang demikian menyebabkan atom karbon dapat membentuk rantai karbon yang sangat panjang dengan ikatan kovalen, baik ikatan kovalen tunggal, rangkap 2, maupun rangkap 3. Selain itu dapat pula membentuk rantai lingkar (siklik).
B. Senyawa Hidrokarbon
Senyawa karbon yang paling sederhana adalah hidrokarbon karena hanya terdiri dari dua unsur, yaitu karbon (C) dan hidrogen (H). Meskipun demikian jumlah senyawa yang dihasilkan dari kedua unsur ini sangat banyak.
Berdasarkan kedudukannya, ada 4 macam atom karbon, yaitu atom karbon primer, sekunder, tersier, dan kuarterner. Keistimewaan atom karbon yang dapat membentuk ikatan kovalen sebanyak 4 buah dan kemampuannya dalam membentuk rantai karbon, menyebabkan atom karbon mempunyai kedudukan yang berbeda-beda.
Kedudukan tersebut adalah:
1. Atom karbon primer, yaitu atom karbon yang terikat langsung pada 1 atom karbon yang lain.
2. Atom karbon sekunder, yaitu atom karbon yang terikat langsung pada 2 atom karbon yang lain.
3. Atom karbon tersier, yaitu atom karbon yang terikat langsung pada 3 atom karbon yang lain.
4. Atom karbon kuarterner, yaitu atom karbon yang terikat langsung pada 4 atom karbon yang lain.
Contoh:
Pada contoh di atas dapat dilihat jumlah atom karbon pada masing-masing posisi,
yaitu:
primer : 5 (yang bertanda 1°)
sekunder : 3 (yang bertanda 2°)
tersier : 1 (yang bertanda 3°)
kuarterner : 1 (yang bertanda 4°)
Isomer
Isomer adalah dua senyawa atau lebih yang mempunyai rumus kimia sama tetapi mempunyai struktur yang berbeda. Secara garis besar isomer dibagi menjadi dua, yaitu isomer struktur, dan isomer geometri.
1. Isomer struktur
Isomer struktur dapat dikelompokkan menjadi: isomer rangka, isomer posisi, dan isomer gugus fungsi.
a. Isomer rangka adalah senyawa-senyawa yang mempunyai rumus molekul sama tetapi kerangkanya berbeda. Contoh pada alkana, alkena, dan alkuna
isomer butana
isomer pentena
isomer pentuna
b. Isomer posisi adalah senyawa-senyawa yang memiliki rumus molekul sama tetapi posisi gugus fungsinya berbeda. Contoh pada alkena dan alkuna.
isomer butena
isomer butuna
c. Isomer gugus fungsi adalah senyawa-senyawa yang mempunyai rumus molekul sama tetapi gugus fungsinya berbeda. Contoh pada alkuna dan alkadiena.
contoh:
2. Isomer geometri
Isomer geometri adalah senyawa-senyawa yang mempunyai rumus molekul sama tetapi struktur ruangnya berbeda. Contoh pada alkena mempunyai 2 isomer geometri yaitu cis dan trans.
C. Penggolongan Hidrokarbon
Penggolongan hidrokarbon didasarkan pada dua hal, yaitu bentuk rantai karbon dan jenis ikatan.
1. Berdasarkan Bentuk Rantai Karbon
a. Rantai karbon alifatis, yaitu rantai karbon terbuka. Rantai karbon alifatis ini bisa lurus dan bisa juga bercabang. Contoh:
b. Rantai karbon siklis, yaitu rantai karbon tertutup. Dibedakan atas karbosiklik dan heterosiklik.
1) Karbosiklik adalah senyawa karbon siklik yang rantai lingkarnya hanya terdiri dari atom C saja. Yang termasuk karbosiklik adalah senyawa aromatis dan alisiklik.
a) Senyawa aromatis adalah senyawa karbosiklik yang terdiri atas 6 atom karbon atau lebih yang memiliki ikatan rangkap 2 terkonjugasi. Contoh:
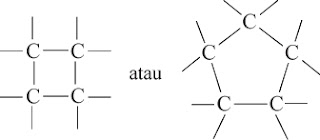
b) Senyawa alisiklik adalah senyawa karbosiklik yang hanya mempunyai ikatan tunggal. Contoh:
2) Heterosiklik adalah senyawa karbosiklik yang di dalam rantai lingkarnya terdapat atom lain selain atom karbon. Contoh:
Berdasarkan Jenis Ikatan
a. Ikatan jenuh, jika semua ikatan karbonnya merupakan ikatan tunggal (– C – C –).
b. Ikatan tak jenuh, jika mengandung ikatan rangkap 2 (– C = C –) maupun rangkap 3 (– C ≡ C –) pada ikatan karbon-karbon. Dikatakan tak jenuh karena ikatan rangkap, baik rangkap 2 maupun rangkap 3 ini masih dapat mengalami pemutusan ikatan. Contoh:
D. Senyawa Alkana, Alkena, dan Alkuna (hidrokarbon alifatis)
1. Alkana
a.Rumus Umum Alkana
Alkana merupakan senyawa hidrokarbon alifatik jenuh, yaitu hidrokarbon dengan rantai terbuka dan semua ikatan karbonnya merupakan ikatan tunggal. Senyawa alkana mempunyai rumus
Pada tabel berikut terdapat nama-nama sepuluh alkana dengan jumlah atom karbon 1 sampai 10. Hal ini merupakan dasar nama-nama senyawa organik.
Dari metana ke etana mempunyai perbedaan –CH2–, begitu pula seterusnya. Deret senyawa karbon dengan gugus fungsi sama dengan selisih sama yaitu –CH2– disebut deret homolog.
b.Gugus Alkil
Gugus alkil adalah alkana yang telah kehilangan satu atom H. Gugus alkil ini dapat dituliskan dengan menggunakan rumus:
CnH2n + 1
Dengan menggantikan satu atom H, maka namanya juga akan berubah dari metana menjadi metil. Berikut ini beberapa gugus alkil yang biasa digunakan.
Gugus metil dan gugus etil masing-masing hanya sejenis, yaitu
Gugus propil ada dua jenis, yaitu:
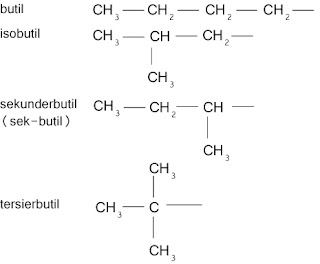
Sedangkan gugus butil ada empat jenis, yaitu:
c. Tata Nama Alkana
Pemberian nama alkana ini akan sangat sulit jika hanya menggunakan tata nama alkana biasa karena adanya isomer-isomer dalam alkana, sehingga perlu adanya nama-nama khusus. Misalnya, awalan normal digunakan untuk rantai lurus, sedangkan awalan iso untuk isomer yang mempunyai satu cabang CH3 yang terikat pada atom karbon nomor dua.
Kemudian pada tahun 1892 perhimpunan kimiawan internasional pada pertemuan di Jenewa telah merumuskan aturan penamaan senyawa kimia. Tata nama yang di rumuskan itu terkenal dengan tata nama IUPAC (International Union of Pure and Applied Chemistry). Nama yang diturunkan dengan aturan ini disebut nama sistematik atau nama IUPAC, sedangkan nama yang sudah biasa digunakan sebelum tata nama IUPAC tetap digunakan dan disebut dengan nama biasa atau nama trivial.
Aturan IUPAC untuk penamaan alkana bercabang sebagai berikut.
1.Alkana rantai lurus diberi nama dengan awalan n (n = normal).
Contoh:
CH3-CH2-CH2-CH3 n-butana
CH3-CH2-CH2-CH2-CH3 n-pentana
2. Alkana rantai bercabang
1) Nama alkana bercabang terdiri dari dua bagian, yaitu:
a) Bagian pertama, di bagian depan, yaitu nama cabang (cabang-cabang).
b) Bagian kedua, di bagian belakang, yaitu nama rantai induk. Contoh:
2) Rantai induk adalah rantai terpanjang dalam molekul. Bila terdapat dua atau lebih rantai terpanjang, maka harus dipilih yang mempunyai cabang terbanyak. Induk diberi nama alkana, tergantung pada panjang rantai.
Contoh:
3) Cabang diberi nama alkil, yaitu nama alkana yang sesuai dengan mengganti akhiran ana menjadi il. Gugus alkil mempunyai rumus umum CnH2n + 1 dan dinyatakan dengan lambang R.
4) Posisi cabang dinyatakan dengan awalan angka. Untuk itu rantai induk perlu dinomori. Penomoran dimulai dari salah satu ujung rantai induk sedemikian hingga posisi cabang mendapat nomor terkecil. Contoh:
5) Jika terdapat dua atau lebih cabang yang sama, hal ini dinyatakan dengan awalan di, tri, tetra, penta, dan seterusnya pada nama cabang.
6) Cabang-cabang yang berbeda disusun sesuai urutan abjad dari nama cabang itu.
Misalnya:
• Etil ditulis terlebih dahulu daripada metil.
• Isopropil ditulis terlebih dahulu daripada metil.
Berdasarkan aturan tersebut, penamaan alkana dapat dilakukan dengan langkah-langkah sebagai berikut.
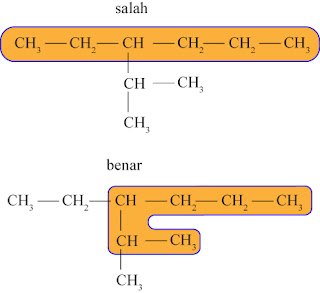
1) Memilih rantai induk, yaitu rantai terpanjang yang mempunyai cabang terbanyak.
2) Memberi penomoran dimulai dari salah satu ujung, sehingga cabang mendapat nomor terkecil.
3) Menuliskan nama dimulai dengan nama cabang yang disusun menurut abjad, kemudian diakhiri dengan nama rantai induk. Posisi cabang dinyatakan dengan awalan angka. Antara angka dengan angka dipisahkan dengan tanda koma (,), sedangkan antara angka dengan huruf dipisahkan tanda jeda (–).
Berikut ini contoh pemberian nama pada alkana.
d. Isomerisasi pada Alkana
Sebagaimana telah kita pelajari di depan bahwa pada senyawa hidrokarbon dikenal istilah isomer. Isomer yang terjadi pada alkana adalah isomer rangka.
Sebagai contoh C5H12 mempunyai isomer:
Artinya, senyawa dengan rumus molekul C5H12 memiliki 3 isomer.
e. Sifat Alkana
1) Semua hidrokarbon merupakan senyawa nonpolar sehingga tidak larut dalam air. Jika suatu hidrokarbon bercampur dengan air, maka lapisan hidrokarbon selalu di atas sebab massa jenisnya lebih kecil daripada 1. Pelarut yang baik untuk hidrokarbon adalah pelarut nonpolar, seperti CCl4 atau eter.
2) Makin banyak atom C, titik didih makin tinggi. Untuk hidrokarbon yang berisomer (jumlah atom C sama banyak), titik didih makin tinggi apabila rantai C makin panjang (bercabang sedikit).
3) Pada suhu dan tekanan biasa, empat alkana yang pertama (CH4 sampai C4H10) berwujud gas. Pentana (C5H12) sampai heptadekana (C17H36) berwujud cair, sedangkan oktadekana (C18H38) dan seterusnya berwujud padat.
4) Jika direaksikan dengan unsur-unsur halogen (F2, Cl2, Br2, dan I2), maka atom-atom H pada alkana mudah mengalami substitusi (penukaran) oleh atom-atom halogen.
5) Alkana dapat mengalami oksidasi dengan gas oksigen, dan reaksi pembakaran ini selalu menghasilkan energi. Itulah sebabnya alkana digunakan sebagai bahan bakar.
6) Senyawa alkana rantai panjang dapat mengalami reaksi eliminasi. Reaksi eliminasi adalah reaksi penghilangan atom/gugus atom untuk memperoleh senyawa karbon lebih sederhana.
2. Alkena
a. Rumus Umum Alkena
Alkena adalah hidrokarbon alifatik tak jenuh yang memiliki satu ikatan rangkap (C = C).
Senyawa yang mempunyai dua ikatan rangkap disebut alkadiena, yang mempunyai tiga ikatan rangkap disebut alkatriena, dan seterusnya.
rumus umum alkena adalah
b. Tata Nama Alkena
1) Alkena rantai lurus
Nama alkena rantai lurus sesuai dengan nama–nama alkana, tetapi dengan mengganti akhiran –ana menjadi –ena.
Contoh:
• C2H4 etena
• C3H6 propena
• C4H8 butena
2) Alkena rantai bercabang Urutan penamaan adalah:
a) Memilih rantai induk, yaitu rantai karbon terpanjang yang mengandung ikatan rangkap.
Contoh:
b) Memberi nomor, dengan aturan penomoran dimulai dari salah satu ujung rantai induk, sehingga ikatan rangkap mendapat nomor terkecil (bukan berdasarkan posisi cabang).
Contoh:
c) Penamaan, dengan urutan:
- nomor atom C yang mengikat cabang
- nama cabang
- nomor atom C ikatan rangkap
- nama rantai induk (alkena)
Contoh:
c. Keisomeran Alkena
Alkena mempunyai dua keisomeran sebagai berikut.
1) Keisomeran Struktur
Keisomeran struktur, yaitu keisomeran yang terjadi jika rumus molekul sama, tetapi rumus struktur berbeda. Keisomeran pada alkena mulai ditemukan pada C4H8 terus ke suku yang lebih tinggi.
contoh:
a) C4H8 mempunyai tiga macam isomer, yaitu:
isoemer pentena
2) Keisomeran Geometri
Keisomeran geometri, yaitu keisomeran yang terjadi karena perbedaan orientasi gugus-gugus di sekitar C ikatan rangkap.
Contoh:
2–butena mempunyai dua isomer geometri, yaitu cis–2–butena dan trans–2–butena.
Syarat terjadinya isomer geometri adalah apabila masing-masing atom karbon yang berikatan rangkap mengikat 2 atom atau 2 gugus yang berbeda, sehingga jika atom atau gugus yang diikat tersebut bertukar tempat, maka strukturnya akan menjadi berbeda.
d. Sifat-sifat Alkena
1) Sifat Fisis
Titik leleh dan titik didih alkena hampir sama dengan alkana yang sesuai. Pada suhu kamar, suku-suku rendah berwujud gas, suku-suku sedang berwujud cair, dan suku-suku tinggi berwujud padat.
2) Reaksi-reaksi Alkena
Alkena jauh lebih reaktif daripada alkana karena adanya ikatan rangkap. Reaksi alkena terutama terjadi pada ikatan rangkap tersebut.
Reaksi-reaksi alkena sebagai berikut.
a) Reaksi Adisi (penambahan atau penjenuhan)
Reaksi adisi, yaitu pengubahan ikatan rangkap menjadi ikatan tunggal dengan cara mengikat atom lain.
Zat-zat yang dapat mengadisi alkena adalah:
(1) Gas hidrogen (H2)
(2) Halogen (F2, Cl2, Br2, dan I2)
(3) Asam halida (HCl, HBr, HF, dan HI)
Jika alkena menangkap asam halida berlaku aturan Markovnikov, yaitu atom H dari asam halida akan terikat pada atom C berikatan rangkap yang telah memiliki atom H lebih banyak.
Contoh:
b) Reaksi Pembakaran (oksidasi dengan oksigen)
Pembakaran sempurna alkena menghasilkan CO2 dan H2O.
Pembakaran tidak sempurna alkena menghasilkan CO dan H2O.
c) Reaksi Polimerisasi
Reaksi polimerisasi adalah reaksi penggabungan molekul-molekul sederhana (monomer) menjadi molekul besar (polimer).
Contoh:
Polimerisasi etena menjadi polietena
3. Alkuna
a. Rumus Umum
Alkuna adalah senyawa hidrokarbon alifatik tak jenuh yang mengandung ikatan rangkap tiga.
rumus umum alkuna adalah:
contoh beberapa alkuna:
b. Tata Nama Alkuna
1) Alkuna rantai lurus namanya sama dengan alkana, hanya akhiran “ana” diganti dengan “una”.
Contoh:
C3H4 = propuna
C4H6 = butuna
C5H8 = pentuna
2) Alkuna rantai bercabang
Urutan penamaan adalah:
a) Memilih rantai induk, yaitu rantai karbon terpanjang yang mengandung ikatan rangkap tiga. Contoh:
b) Penomoran alkuna dimulai dari salah satu ujung rantai induk, sehingga atom C yang berikatan rangkap tiga mendapat nomor terkecil. Contoh:
c) Penamaan, dengan urutan:
• nomor C yang mengikat cabang
• nama cabang
• nomor C yang berikatan rangkap tiga
• nama rantai induk (alkuna)
Contoh:
c. Keisomeran Alkuna
Alkuna hanya mempunyai keisomeran struktur, tidak mempunyai keisomeran geometri. Keisomeran alkuna dimulai dari C4H6.
Contoh:
1) C4H6 mempunyai dua isomer, yaitu:
d. Sifat-sifat Alkuna
1) Sifat Fisis
Sifat fisis alkuna sama dengan sifat fisis alkana maupun alkena.
2) Sifat Kimia (Reaksi Alkuna)
Reaksi- reaksi pada alkuna mirip dengan alkena, hanya berbeda pada kebutuhan jumlah pereaksi untuk penjenuhan ikatan rangkap. Alkuna membutuhkan jumlah pereaksi dua kali kebutuhan pereaksi pada alkena untuk jumlah ikatan rangkap yang sama.
contoh:




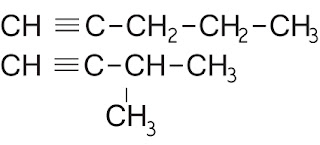










































EmoticonEmoticon